België: ondervoeding bij kankerpatiënten onderschat
04 Jul 2024
De studie ONCOCARE schetst de situatie van ondervoeding bij de oncologische patiënten in de Belgische ziekenhuizen: 1 op de 4 patiënten is ondervoed bij de opstart van een kankerbehandeling en 1 op de 2 patiënten raakt tijdens die behandeling ondervoed. Snel actie ondernemen is de boodschap.
Ondervoeding – veelvoorkomend bij kankerpatiënten – brengt heel wat gevolgen met zich mee. Patiënten verdragen de chemotherapie minder goed, reageren minder goed op de behandeling tegen kanker, het risico op complicaties is groter, de postoperatieve resultaten zijn minder gunstig, de patiënten blijven langer in het ziekenhuis en hun levenskwaliteit verslechtert. Uiteindelijk leidt ondervoeding tot een verhoogd risico op overlijden[1]. Ondervoeding is vooral het gevolg van een combinatie van anorexia en een verstoord metabolisme als gevolg van de tumor zelf en/of de kankerbehandelingen (chemotherapie, radiotherapie, …). Het onbedoelde gewichtsverlies wordt ook in de hand gewerkt door fysiologische veranderingen, inherent aan de kanker, die kunnen leiden tot een slechte voedselopname, diarree en braken[2].
Ondervoedingscijfers in Europa
Recente studies schatten de prevalentie van ondervoeding bij kankerpatiënten tussen de 36 % en 50%[3]. De dieetbehandeling op de dienst oncologie bestaat in eerste instantie uit het gebruik van een gevalideerd meetinstrument voor de opsporing van ondervoeding, zoals aanbevolen door ESPEN. De Nutritional Risk Screening (NRS- 2002)[4], bijvoorbeeld. Wat is de status in België? Uiteraard zijn er geen epidemiologische cijfers over ondervoeding bij kankerpatiënten voorhanden. De klinische praktijken voor de opsporing, evaluatie en dieetbehandeling lijken ook sterk te verschillen van centrum tot centrum. Dit heeft een groep onderzoekers van verschillende ziekenhuizen uit ons land aangezet om een studie uit te voeren. De eerste doelstelling van ONCOCARE is om prevalentie van ondervoeding op prospectieve wijze in kaart brengen bij patiënten met solide tumoren die een neoadjuvante kankerbehandeling of een eerste-, tweede- of derdelijns behandeling voor een metastatische kanker met palliatieve doeleinden opstarten[5].
Risico op ondervoeding bij meer dan een op de twee patiënten
Ondervoeding werd opgespoord met de NRS-2002 en op basis van het Global Leadership Initiative on Malnutrition (GLIM) gediagnosticeerd[6]. De onderzoekers hebben eveneens de aanwezigheid van sarcopenie onderzocht op basis van de verklaringen aangaande kracht, stapvermogen, rechtstaan uit zithouding, trappen lopen en neiging tot vallen. De studie werd uitgevoerd bij een totaal van 328 patiënten die na start van behandeling tijdens twee consultaties werden opgevolgd. Het eerste bezoek vond plaats na 6 weken behandeling en het tweede na 4 maanden (Figuur 1).

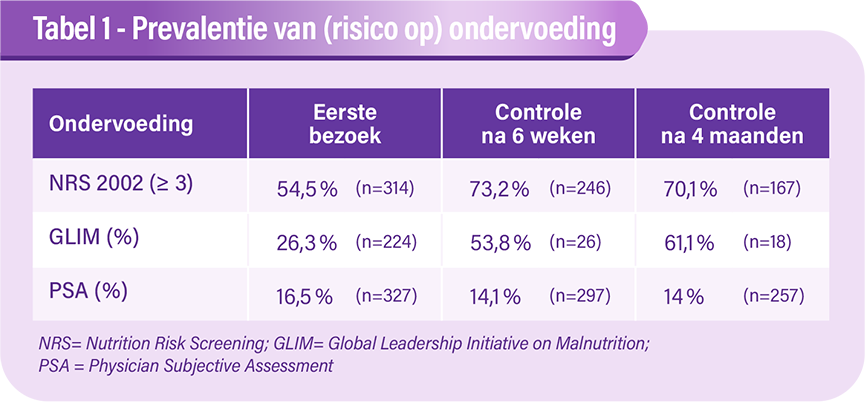
De resultaten wijzen op een hoge prevalentie van ondervoeding. Tijdens de eerste consultatie, bijna 4 weken na de opstart van de kankerbehandeling, had 54,5 % van de patiënten een NRS van meer dan 3. Dit wijst op een risico op ondervoeding. Deze verhouding is gestegen in de loop van de opvolgingsperiode, met uiteindelijk 73,2 % tijdens de eerste opvolgingsconsultatie (ongeveer 6 weken na de opstart van de kankerbehandeling). Tijdens de 2e opvolgingsconsultatie, ongeveer 4 maanden na de opstart van die behandeling, bedroeg de prevalentie van ondervoeding zo’n 70,1 % (Tabel 1).
Op basis van de GLIM-criteria is er sprake van ondervoeding bij 26,3 % van de patiënten bij start van de behandeling. Deze cijfers stegen ook in de loop van de opvolging, tot 53,8 % na 6 weken en 61,1 % na 4 maanden. Bovendien melden de auteurs dat de prevalentie van subjectief door de oncoloog beoordeelde gevallen van ondervoeding lager ligt dan de resultaten van de NRS-2002 en de GLIM-score, en dit bij elk van de 3 bezoeken (Tabel 1).
Opvallend energietekort
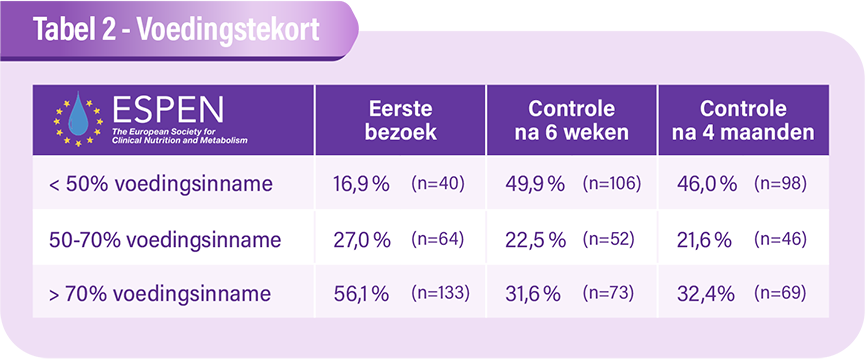
Volgens de aanbevelingen van ESPEN (calorie-inname van 30 kcal/kg/dag) stelden de onderzoekers vanaf de opstart van de kankerbehandeling een gemiddeld tekort van 500 kcal vast. Een calorietekort dat na verloop van tijd erger wordt: 980 kcal na 6 weken kankerbehandeling en 990 kcal na 4 maanden.
Het percentage patiënten met een energie-inname onder 50% van de behoefte steeg van 16,9% bij het eerste bezoek naar 49,9% na 6 weken en 46% na 4 maanden (tabel 2). Bij aanvang van de behandeling vertonen meer dan 4 op de 10 patiënten (43,9 %) een voedingstekort van minder dan 70 % van hun behoeften (tabel 2). Conform de aanbevelingen van ESPEN bij kankerpatiënten zou er al medische drinkvoeding bij deze kankerpatiënten aanbevolen moeten worden. Ongeveer 1 op de 7 mensen (12,4 % bij het 1e bezoek, 15,5 % bij het 2e opvolgingsbezoek) leed aan sarcopenie. Bij meer dan 1 op de 3 patiënten werd cachexie vastgesteld (38,1 % bij het 1e bezoek, 37,7 % bij het 2e opvolgingsbezoek). Het is niet verwonderlijk dat sarcopenie en cachexie vaker voorkomen bij de mensen die tijdens het 1e bezoek al een risico op ondervoeding vertoonden.
Voeding speelt duidelijk een cruciale rol in de behandeling van kankerpatiënten. Het is dan ook belangrijk zo snel mogelijk een gepersonaliseerd voedingsplan voor hen op te stellen. Hierbij moet men niet enkel rekening houden met de specifieke behoeften van de patiënt, het soort/stadium van de kanker, het behandelplan en de eventuele bijwerkingen, maar ook met de initiële voedingstoestand van de patiënt. Het is van essentieel belang dat men toeziet op een voldoende hoge calorie-inname om het lichaamsgewicht en de spiermassa op peil te houden en de patiënt te helpen om in te spelen op de hogere energiebehoeftes die de kanker zelf met zich meebrengt. Niet alleen moet men de inname van hoogwaardige eiwitten via de voeding verhogen (mager vlees, vis, eieren, zuivelproducten, peulvruchten enz.), maar de voeding ook aanpassen aan de bijwerkingen waarmee de patiënt te maken krijgt. Wanneer het moeilijk is om enkel met voeding aan de behoeften te voldoen, is het gebruik van voedingssupplementen sterk – en zo snel mogelijk – aanbevolen.
Deze studie bevestigt dat ondervoeding in België, net als in andere landen, te weinig wordt gediagnosticeerd bij kankerpatiënten. De auteurs besluiten dat de vroegtijdige opsporing van voedingstekorten en een aanpassing van de voedselinname meteen na de opstart van alle mogelijke kankerbehandelingen zou kunnen leiden tot betere klinische resultaten bij de patiënten met kanker.
[1] Bossi P et al. Malnutrition management in oncology: An expert view on controversial issues and future perspectives. Front Oncol 2022;12:910770. [2] Hébuterne X et al. Prevalence of malnutrition and current use of nutrition support in patients with cancer. J Parenter Enteral Nutr 2014;38(2):196–204. [3] Marshall et al. Prevalence of manutrition and impact on clinical outcomes in cancer services:a comparison of two timepoints. Clin Nutr 2019;38(2):644–651. [4] Muscaritoli et al. ESPEN practical guidelines : clinical nutrition in cancer. Clin Nutr 2021;40:2898–2913. [5] Rasschaert M et al. Malnutrition prevalence in cancer patients in Belgium: The ONCOCARE Study. Support Care Cancer 2024;32:35. [6] Cederholm et al. GLIM criteria for the diagnosis of malnutrition – a consensus report from the global clinical nutrition community; ESPEN endorsed recommendations. Clin Nutr 2017;36(1):7–10.